喜讯|我院顺利通过国家药物临床试验机构(GCP)资格认定
阅读量
·
2017-05-17
厦门大学附属厦门眼科中心于2014年申报国家药物临床试验机构,今年3月接受了国家食品药品监督管理局委派福建省食品药品监督管理局进行的药物临床试验机构资格(GCP)认定现场检查。

专家组对厦门眼科中心进行了现场检查和考核,详细了解眼科专业的急救设施与研究条件,重点考核了医院药物临床试验机构、临床试验伦理委员会以及专业研究团队、设施设备、管理制度以及SOP标准操作规程,并现场就眼科专业在实施GCP中可能遇到的伦理和技术问题进行了深入交流,最后出具了综合评定意见。

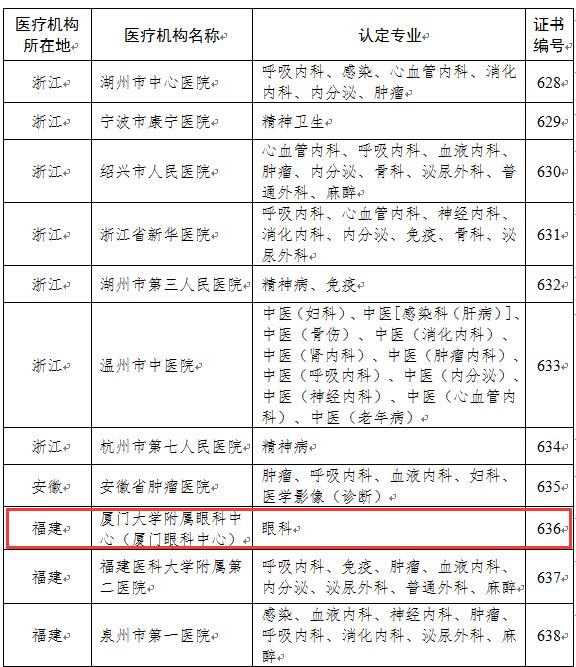
根据《药物临床试验质量管理规范》、《药品注册管理办法》《药物临床试验机构资格认定办法》,经资料审查和现场检查,厦门大学附属厦门眼科中心于2017年5月15日由国家食品药品监督管理总局发布的《药物临床试验机构资格认定公告》(第7号)(2017年第57号),通告我院药物临床试验机构顺利通过国家GCP资格认定,予以颁发《药物临床试验机构资格认定证书》。
什么是GCP?
GCP是“药物临床试验管理规范”的英文简称,指规范药物临床试验全过程的标准规定,其目的在于保证临床试验过程的规范,结果科学可靠,保护受试者的权益。

GCP是在充分保护受试者、伦理委员会通过基础上制定的新药上市前的临床研究阶段,为临床疑难耐药患者提供了新的治疗选择途径。

药物临床试验是确证新药有效性必不可少的步骤,进行药物临床试验需要多种专业技术人员的合作。一个好的临床研究队伍不仅应包括医学、药学、药理学、生物学、生物统计学等专业人员,还应包括非医学专业的但富有经验的文档管理人员。获得药物临床试验资格,是一所医院医疗水平和科研能力的综合体现,标志着厦门眼科中心已达到国家规定的药物临床试验水平。

厦门眼科中心将以此为契机,细致、扎实地做好各类各期临床试验工作,促进我院药物临床试验走向新的发展阶段。厦门眼科中心李晓峰院长表示,通过机构认定只是万里长征的开始,我们一定要按照GCP的流程规范、结构科学合理、确保受试者的要求去做,认定通过只是开端、起点,努力永无止境!


 医院概况
医院概况 就诊科室
就诊科室 就诊指南
就诊指南



